Měrná tepelná kapacita je 240. Můžete také vyjádřit z tohoto vzorce
Změna vnitřní energie vykonáváním práce je charakterizována množstvím práce, tzn. práce je mírou změny vnitřní energie v daném procesu. Změna vnitřní energie tělesa při přenosu tepla je charakterizována veličinou nazývanou množství tepla.
je změna vnitřní energie tělesa při procesu přenosu tepla bez vykonání práce. Množství tepla je označeno písmenem Q .
Práce, vnitřní energie a teplo se měří ve stejných jednotkách – joulech ( J), jako každý druh energie.
Při tepelných měřeních se dříve jako jednotka množství tepla používala speciální jednotka energie - kalorie ( výkaly), rovná se množství tepla potřebného k ohřátí 1 gramu vody o 1 stupeň Celsia (přesněji od 19,5 do 20,5 °C). Zejména tato jednotka se v současnosti používá při výpočtu spotřeby tepla (tepelné energie) v bytových domech. Experimentálně byl stanoven mechanický ekvivalent tepla - vztah mezi kaloriemi a jouly: 1 kal = 4,2 J.
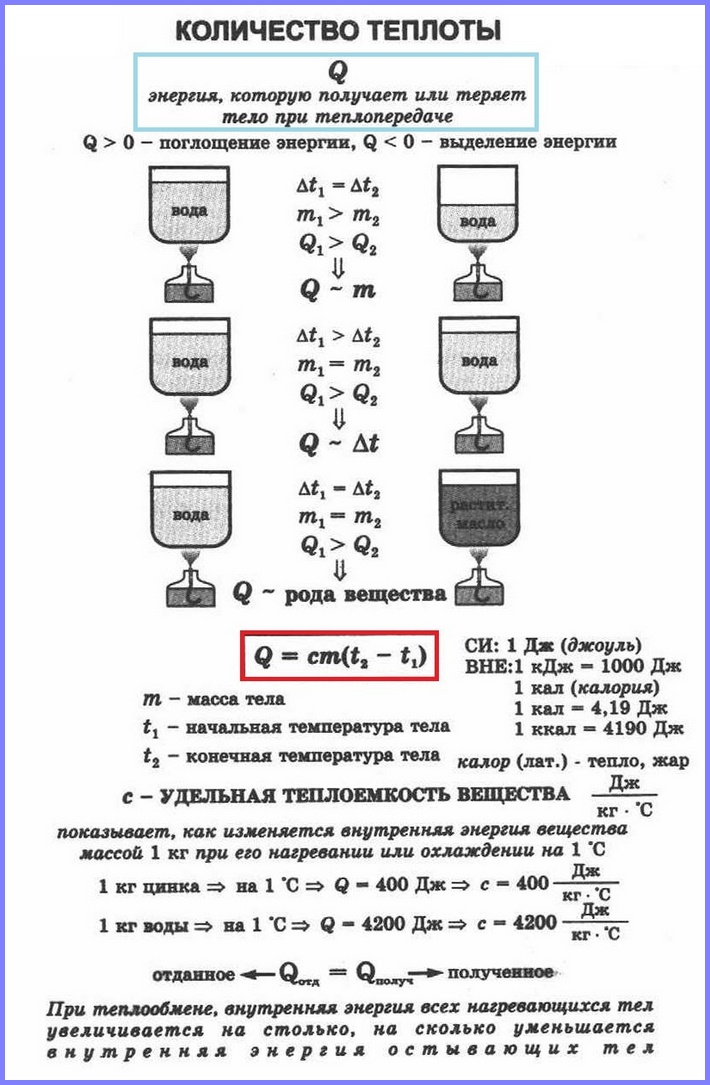
Když tělo předá určité množství tepla, aniž by vykonalo práci, jeho vnitřní energie se zvýší, pokud tělo vydá určité množství tepla, pak se jeho vnitřní energie sníží.
Pokud nalijete 100 g vody do dvou stejných nádob, jedné a 400 g do druhé o stejné teplotě a postavíte je na stejné hořáky, pak se voda v první nádobě uvaří dříve. Čím větší je tedy tělesná hmota, tím větší množství tepla potřebuje k zahřátí. Stejné je to s chlazením.

Množství tepla potřebného k zahřátí tělesa závisí také na typu látky, ze které je těleso vyrobeno. Tuto závislost množství tepla potřebného k zahřátí tělesa na druhu látky charakterizuje fyzikální veličina tzv měrná tepelná kapacita látek.
je fyzikální veličina rovnající se množství tepla, které musí být předáno 1 kg látky, aby se zahřálo o 1 °C (nebo 1 K). 1 kg látky uvolní stejné množství tepla při ochlazení o 1 °C.
Měrná tepelná kapacita je označena písmenem S. Jednotkou měrné tepelné kapacity je 1 J/kg °C nebo 1 J/kg °K.
Měrná tepelná kapacita látek se zjišťuje experimentálně. Kapaliny mají vyšší měrnou tepelnou kapacitu než kovy; Voda má nejvyšší měrné teplo, zlato má velmi malé měrné teplo.
Protože se množství tepla rovná změně vnitřní energie tělesa, můžeme říci, že měrná tepelná kapacita ukazuje, jak moc se mění vnitřní energie 1 kg látky, když se její teplota mění o 1 °C. Zejména vnitřní energie 1 kg olova se při zahřátí o 1 °C zvýší o 140 J a při ochlazení se sníží o 140 J.
Q potřebné k zahřátí hmotného tělesa m na teplotě t 1 °C až do teploty t 2 °С, se rovná součinu měrné tepelné kapacity látky, tělesné hmotnosti a rozdílu mezi konečnou a počáteční teplotou, tzn.Q = c ∙ m (t 2 - t 1)
Stejný vzorec se používá k výpočtu množství tepla, které tělo vydává při ochlazování. Pouze v tomto případě by měla být konečná teplota odečtena od počáteční teploty, tzn. Odečtěte nižší teplotu od vyšší teploty.

Toto je shrnutí tématu „Množství tepla. Specifické teplo". Vyberte, co dělat dál:
- Přejít na další shrnutí:
Měrná tepelná kapacita je vlastnost látky. To znamená, že pro různé látky je to různé. Navíc stejná látka, ale v různých stavech agregace, má různou měrnou tepelnou kapacitu. Správně je tedy hovořit o měrné tepelné kapacitě látky (měrná tepelná kapacita vody, měrná tepelná kapacita zlata, měrná tepelná kapacita dřeva atd.).
Měrná tepelná kapacita konkrétní látky ukazuje, jaké množství tepla (Q) jí musí být předáno, aby se 1 kilogram této látky ohřál o 1 stupeň Celsia. Měrná tepelná kapacita se označuje latinským písmenem c. To znamená, že c = Q/mt. Uvážíme-li, že t a m se rovnají jednotce (1 kg a 1 °C), pak se měrná tepelná kapacita číselně rovná množství tepla.
Teplo a měrná tepelná kapacita však mají různé jednotky měření. Teplo (Q) v Cu systému se měří v joulech (J). A měrná tepelná kapacita je v joulech dělená kilogramem násobená stupni Celsia: J/(kg °C).
Pokud je měrná tepelná kapacita látky např. 390 J/(kg °C), znamená to, že pokud se 1 kg této látky zahřeje o 1 °C, přijme 390 J tepla. Nebo jinými slovy, aby se 1 kg této látky zahřál o 1 °C, musí se jí předat 390 J tepla. Nebo pokud se 1 kg této látky ochladí o 1 °C, vydá 390 J tepla.
Pokud se ne 1, ale 2 kg látky ohřeje o 1 °C, musí se jí předat dvojnásobek tepla. Takže pro příklad výše to bude již 780 J. Totéž se stane, pokud se 1 kg látky zahřeje o 2 °C.
Měrná tepelná kapacita látky nezávisí na její počáteční teplotě. To znamená, že pokud má např. kapalná voda měrnou tepelnou kapacitu 4200 J/(kg °C), pak ohřev o 1 °C i dvacetistupňové nebo devadesátistupňové vody bude stejně vyžadovat 4200 J tepla na 1 kg. .
Ale led má specifickou tepelnou kapacitu, která se liší od kapalné vody, téměř dvakrát menší. K ohřátí o 1 °C však bude potřeba stejné množství tepla na 1 kg bez ohledu na jeho počáteční teplotu.
Měrná tepelná kapacita také nezávisí na tvaru tělesa, které je z této látky vyrobeno. Ocelová tyč a ocelový plech mající stejnou hmotnost budou vyžadovat stejné množství tepla, aby se zahřály o stejný počet stupňů. Další věc je, že je třeba zanedbávat výměnu tepla s okolím. Plech má větší povrch než tyč, což znamená, že plech vydává více tepla, a proto se rychleji ochladí. Ale za ideálních podmínek (kdy lze ztráty tepla zanedbat) na tvaru těla nezáleží. Proto říkají, že měrná tepelná kapacita je charakteristikou látky, ale ne tělesa.
Měrná tepelná kapacita různých látek je tedy různá. To znamená, že pokud jsou dány různé látky se stejnou hmotností a stejnou teplotou, tak aby se zahřály na jinou teplotu, musí se jim předat různé množství tepla. Například kilogram mědi bude vyžadovat asi 10krát méně tepla než voda. To znamená, že měď má specifickou tepelnou kapacitu, která je přibližně 10krát menší než kapacita vody. Můžeme říci, že „do mědi je umístěno méně tepla“.
Množství tepla, které musí být tělu předáno, aby se zahřálo z jedné teploty na druhou, se zjistí pomocí následujícího vzorce:
Q = cm(t k – t n)
Zde tk a tn jsou konečné a počáteční teploty, m je hmotnost látky, c je její měrná tepelná kapacita. Měrná tepelná kapacita se obvykle přebírá z tabulek. Z tohoto vzorce lze vyjádřit měrnou tepelnou kapacitu.
Fyzika a tepelné jevy je poměrně rozsáhlá sekce, která je důkladně studována ve školním kurzu. Konkrétním veličinám není v této teorii věnováno poslední místo. První z nich je měrná tepelná kapacita.
Výkladu slova „specifický“ se však obvykle nevěnuje dostatečná pozornost. Studenti si to prostě pamatují jako samozřejmost. co to znamená?
Pokud se podíváte do Ozhegovova slovníku, můžete si přečíst, že takové množství je definováno jako poměr. Navíc to může být provedeno ve vztahu k hmotnosti, objemu nebo energii. Všechna tato množství musí být rovna jedné. S čím souvisí měrná tepelná kapacita?
Na součin hmotnosti a teploty. Kromě toho se jejich hodnoty musí rovnat jedné. To znamená, že dělitel bude obsahovat číslo 1, ale jeho rozměr bude kombinovat kilogram a stupeň Celsia. To je třeba vzít v úvahu při formulaci definice měrné tepelné kapacity, která je uvedena o něco níže. Existuje také vzorec, ze kterého je zřejmé, že tyto dvě veličiny jsou ve jmenovateli.
Co je to?
Měrná tepelná kapacita látky se zavádí v okamžiku, kdy se uvažuje o situaci s jejím ohřevem. Bez něj není možné vědět, kolik tepla (nebo energie) bude pro tento proces zapotřebí. A také vypočítat jeho hodnotu, když se tělo ochladí. Mimochodem, tato dvě množství tepla se navzájem rovnají v modulu. Ale mají různá znamení. Takže v prvním případě je to pozitivní, protože energii je potřeba vydat a ta se přenese do těla. Druhá ochlazovací situace dává záporné číslo, protože se uvolňuje teplo a vnitřní energie těla klesá.
Tato fyzikální veličina se označuje latinským písmenem c. Je definována jako určité množství tepla potřebné k zahřátí jednoho kilogramu látky o jeden stupeň. Ve školním kurzu fyziky je tento stupeň dosažen na stupnici Celsia.

Jak to spočítat?
Pokud chcete vědět, jaká je měrná tepelná kapacita, vzorec vypadá takto:
c = Q / (m * (t 2 - t 1)), kde Q je množství tepla, m je hmotnost látky, t 2 je teplota, kterou těleso získalo v důsledku výměny tepla, t 1 je počáteční teplota látky. Toto je formule číslo 1.
Na základě tohoto vzorce se jednotka měření této veličiny v mezinárodní soustavě jednotek (SI) ukáže jako J/(kg*ºС).
Jak zjistit další veličiny z této rovnosti?
Za prvé, množství tepla. Vzorec bude vypadat takto: Q = c * m * (t 2 - t 1). Pouze je nutné dosadit hodnoty v jednotkách SI. Tedy hmotnost v kilogramech, teplota ve stupních Celsia. Toto je vzorec číslo 2.
Za druhé, hmotnost látky, která se ochlazuje nebo zahřívá. Vzorec pro to bude: m = Q / (c * (t 2 - t 1)). Toto je vzorec číslo 3.
Za třetí, změna teploty Δt = t2 - t1 = (Q / c * m). Znak „Δ“ se čte jako „delta“ a označuje změnu veličiny, v tomto případě teploty. Formule č. 4.
Za čtvrté, počáteční a konečná teplota látky. Vzorce platné pro zahřívání látky vypadají takto: t 1 = t 2 - (Q / c * m), t 2 = t 1 + (Q / c * m). Tyto vzorce jsou č. 5 a 6. Pokud se problém týká ochlazení látky, pak vzorce jsou: t 1 = t 2 + (Q / c * m), t 2 = t 1 - (Q / c * m) . Tyto vzorce jsou č. 7 a 8.

Jaké to může mít významy?
Experimentálně bylo stanoveno, jaké hodnoty má pro každou konkrétní látku. Proto byla vytvořena speciální tabulka měrné tepelné kapacity. Nejčastěji obsahuje data, která jsou platná za normálních podmínek.
Co obnáší laboratorní práce při měření měrné tepelné kapacity?
Ve školním kurzu fyziky je definováno pro pevné těleso. Navíc je jeho tepelná kapacita vypočítána srovnáním s tou, která je známá. Nejjednodušší způsob, jak to udělat, je pomocí vody.

Při práci je nutné měřit počáteční teploty vody a ohřáté pevné látky. Poté jej ponořte do kapaliny a počkejte na tepelnou rovnováhu. Celý experiment se provádí v kalorimetru, takže energetické ztráty lze zanedbat.
Pak musíte napsat vzorec pro množství tepla, které voda přijímá při zahřívání od pevné látky. Druhý výraz popisuje energii, kterou těleso vydává při ochlazování. Tyto dvě hodnoty jsou stejné. Pomocí matematických výpočtů zbývá určit měrnou tepelnou kapacitu látky, která tvoří pevnou látku.
Nejčastěji se navrhuje porovnat jej s tabulkovými hodnotami, aby se pokusilo uhodnout, z jaké látky je studované tělo vyrobeno.
Úkol č. 1
Stav. Teplota kovu se pohybuje od 20 do 24 stupňů Celsia. Zároveň se jeho vnitřní energie zvýšila o 152 J. Jaké je měrné teplo kovu, je-li jeho hmotnost 100 gramů?
Řešení. K nalezení odpovědi budete muset použít vzorec napsaný pod číslem 1. Jsou tam všechna množství potřebná pro výpočty. Nejprve je třeba převést hmotnost na kilogramy, jinak bude odpověď špatná. Protože všechna množství musí být přijata v SI.
V jednom kilogramu je 1000 gramů. To znamená, že 100 gramů je třeba vydělit 1000, dostanete 0,1 kilogramu.
Dosazením všech veličin vznikne následující výraz: c = 152 / (0,1 * (24 - 20)). Výpočty nejsou nijak zvlášť obtížné. Výsledkem všech akcí je číslo 380.
Odpověď: s = 380 J/(kg * ºС).

Problém č. 2
Stav. Určete konečnou teplotu, na kterou se ochladí voda o objemu 5 litrů, pokud byla odebrána při 100 ºС a do okolí uvolnila 1680 kJ tepla.
Řešení. Stojí za to začít s tím, že energie je dána v nesystémové jednotce. Kilojouly je třeba převést na jouly: 1680 kJ = 1680000 J.
Chcete-li najít odpověď, musíte použít vzorec číslo 8. Objevuje se v něm však hmotnost a v problému je neznámá. Ale objem kapaliny je dán. To znamená, že můžeme použít vzorec známý jako m = ρ * V. Hustota vody je 1000 kg/m3. Ale zde bude nutné objem nahradit v metrech krychlových. Chcete-li je převést z litrů, musíte je vydělit 1000. Objem vody je tedy 0,005 m 3 .
Dosazením hodnot do hmotnostního vzorce vznikne následující výraz: 1000 * 0,005 = 5 kg. Měrnou tepelnou kapacitu si budete muset vyhledat v tabulce. Nyní můžete přejít na vzorec 8: t 2 = 100 + (1680000 / 4200 * 5).
První akcí je násobení: 4200 * 5. Výsledek je 21 000. Druhým je dělení. 1680000: 21000 = 80. Poslední je odečítání: 100 - 80 = 20.
Odpověď. t2 = 20 °С.

Problém č. 3
Stav. V kádince o hmotnosti 100 g se nalije 50 g vody. Počáteční teplota vody se sklenicí je 0 stupňů Celsia. Kolik tepla je potřeba k přivedení vody k varu?
Řešení. Dobrým začátkem je zavedení vhodného označení. Nechte údaje týkající se skla mít index 1 a pro vodu - index 2. V tabulce musíte najít konkrétní tepelné kapacity. Kádinka je vyrobena z laboratorního skla, takže její hodnota c 1 = 840 J/ (kg * ºC). Údaje pro vodu jsou: c 2 = 4200 J/ (kg * ºС).
Jejich hmotnosti jsou uvedeny v gramech. Musíte je převést na kilogramy. Hmotnosti těchto látek budou označeny následovně: m 1 = 0,1 kg, m 2 = 0,05 kg.
Počáteční teplota je dána: t 1 = 0 ºС. O konečné hodnotě je známo, že odpovídá bodu, ve kterém se voda vaří. To je t 2 = 100 ºС.
Protože se sklenice zahřívá spolu s vodou, požadované množství tepla bude součet dvou. První, která je nutná k ohřevu skla (Q 1), a druhá, která se používá k ohřevu vody (Q 2). K jejich vyjádření budete potřebovat druhý vzorec. Musí se zapsat dvakrát s různými indexy a pak je sečíst.
Ukazuje se, že Q = c 1 * m 1 * (t 2 - t 1) + c 2 * m 2 * (t 2 - t 1). Společný faktor (t 2 - t 1) může být vyjmut ze závorky, aby byl snazší výpočet. Potom vzorec, který bude vyžadován pro výpočet množství tepla, bude mít následující tvar: Q = (c 1 * m 1 + c 2 * m 2) * (t 2 - t 1). Nyní můžete nahradit veličiny známé v úloze a vypočítat výsledek.
Q = (840 * 0,1 + 4200 * 0,05) * (100 - 0) = (84 + 210) * 100 = 294 * 100 = 29 400 (J).
Odpověď. Q = 29400 J = 29,4 kJ.
Převodník délky a vzdálenosti Převodník hmotnosti Převodník objemových měr sypkých produktů a potravinářských výrobků Převodník ploch Převodník objemu a měrných jednotek v kuchařských receptech Převodník teploty Převodník tlaku, mechanického namáhání, Youngova modulu Převodník energie a práce Převodník výkonu Převodník síly Převodník času Lineární převodník otáček Plochý úhel Převodník tepelná účinnost a palivová účinnost Převodník čísel v různých číselných soustavách Převodník jednotek měření množství informací Kurzy měn Dámské velikosti oblečení a obuvi Velikosti oblečení a obuvi pánské Měnič úhlové rychlosti a frekvence otáčení Měnič zrychlení Měnič úhlového zrychlení Měnič hustoty Měnič měrného objemu Moment měniče setrvačnosti Moment měniče síly Měnič točivého momentu Měrné teplo spalovacího měniče (hmotnostně) Hustota energie a měrné teplo spalovacího měniče (objemově) Převodník teplotního rozdílu Koeficient měniče tepelné roztažnosti Měnič tepelného odporu Konvertor tepelné vodivosti Konvertor měrné tepelné kapacity Konvertor energie a tepelného záření Konvertor hustoty tepelného toku Konvertor součinitele přenosu tepla Konvertor objemového průtoku Konvertor hmotnostního průtoku Konvertor molárního průtoku Konvertor hmotnostní hustoty Konvertor molární koncentrace Konvertor hmotnostní koncentrace v konvertoru roztoku Dynamický (absolutní) převodník viskozity Kinematický převodník viskozity Převodník povrchového napětí Převodník paropropustnosti Převodník paropropustnosti a rychlosti přenosu páry Převodník úrovně zvuku Převodník citlivosti mikrofonu Převodník hladiny akustického tlaku (SPL) Převodník hladiny akustického tlaku s volitelným referenčním tlakem Převodník jasu Převodník světelné intenzity Převodník jasu Počítačová grafika Převodník osvětlení Převodník frekvence a vlnové délky Dioptrický výkon a ohnisková vzdálenost Dioptrický výkon a zvětšení objektivu (×) Převodník elektrického náboje Převodník lineární hustoty náboje Převodník hustoty povrchového náboje Převodník hustoty objemového náboje Převodník hustoty lineárního proudu Převodník hustoty povrchového proudu Převodník intenzity elektrického pole Elektrostatický potenciál a měnič napětí Elektrický odporový měnič Elektrický odporový měnič Měnič elektrické vodivosti Měnič elektrické vodivosti Elektrická kapacita Měnič indukčnosti Americký měnič měřidel drátu Úrovně v dBm (dBm nebo dBm), dBV (dBV), wattech atd. jednotky Magnetomotorický měnič síly Převodník síly magnetického pole Převodník magnetického toku Převodník magnetické indukce Záření. Konvertor dávkového příkonu absorbovaného ionizujícího záření Radioaktivita. Konvertor radioaktivního rozpadu Radiace. Převodník expozičních dávek Radiace. Převodník absorbované dávky Převodník desetinné předpony Přenos dat Převodník jednotek typografie a zpracování obrazu Převodník jednotek objemu dřeva Výpočet molární hmotnosti D. I. Mendělejevova periodická tabulka chemických prvků
Počáteční hodnota
Převedená hodnota
joule na kilogram na kelvin joule na kilogram na °C joule na gram na °C kilojoule na kilogram na kelvin kilojoule na kilogram na °C kalorie (IT) na gram na °C kalorie (IT) na gram na °F kalorie ( term. ) na gram na °C kilokalorie (int.) na kg na °C kalorie (term.) na kg na °C kilokalorie (int.) na kg na kelvin kilokalorie (int.) na kg na kelvin kgf-metr na kilogram na kelvin libra-silová stopa na libru na °Rankine BTU (int.) na libru na °F BTU (term.) na libru na °F BTU (int.) na libru na °Rankine BTU (int.) na libru na °Rankine BTU (int.) na libru na °C za tepla. jednotek za libru na °C
Hmotnostní koncentrace v roztoku
Více o měrné tepelné kapacitě
Obecné informace
Molekuly se pohybují vlivem tepla – tento pohyb se nazývá molekulární difúze. Čím vyšší je teplota látky, tím rychleji se molekuly pohybují a dochází k intenzivnější difúzi. Pohyb molekul ovlivňuje nejen teplota, ale také tlak, viskozita látky a její koncentrace, difúzní odpor, vzdálenost, kterou molekuly při pohybu urazí, a jejich hmotnost. Pokud například porovnáme, jak probíhá proces difúze ve vodě a v medu, když jsou všechny ostatní proměnné kromě viskozity stejné, je zřejmé, že molekuly ve vodě se pohybují a difundují rychleji než v medu, protože med má vyšší viskozitu.
Molekuly potřebují energii k pohybu a čím rychleji se pohybují, tím více energie potřebují. Teplo je v tomto případě jedním z druhů energie. To znamená, že pokud v látce udržujete určitou teplotu, molekuly se budou pohybovat, a pokud se teplota zvýší, pak se pohyb zrychlí. Energie ve formě tepla se získává spalováním paliv, jako je zemní plyn, uhlí nebo dřevo. Pokud zahřejete více látek pomocí stejného množství energie, některé látky se pravděpodobně zahřejí rychleji než jiné v důsledku větší difúze. Tepelná kapacita a měrná tepelná kapacita popisují právě tyto vlastnosti látek.
Specifické teplo určuje, kolik energie (tj. tepla) je potřeba ke změně teploty tělesa nebo látky o určité hmotnosti o určité množství. Tato vlastnost se liší od tepelná kapacita, která určuje množství energie potřebné ke změně teploty celého tělesa nebo látky na určitou teplotu. Při výpočtech tepelné kapacity se na rozdíl od měrné tepelné kapacity nebere v úvahu hmotnost. Tepelná kapacita a měrná tepelná kapacita se počítá pouze pro látky a tělesa ve stabilním stavu agregace, např. pro pevné látky. Tento článek pojednává o obou těchto konceptech, protože spolu souvisí.
Tepelná kapacita a měrná tepelná kapacita materiálů a látek
Kovy

Kovy mají velmi silnou molekulární strukturu, protože vzdálenost mezi molekulami v kovech a jiných pevných látkách je mnohem menší než v kapalinách a plynech. Díky tomu se molekuly mohou pohybovat pouze na velmi krátké vzdálenosti, a proto, aby se mohly pohybovat vyšší rychlostí, je potřeba mnohem méně energie než u molekul kapalin a plynů. Díky této vlastnosti je jejich měrná tepelná kapacita nízká. To znamená, že je velmi snadné zvýšit teplotu kovu.
Voda

Na druhou stranu má voda velmi vysokou měrnou tepelnou kapacitu, a to i ve srovnání s jinými kapalinami, takže na ohřátí jedné jednotky hmotnosti vody o jeden stupeň je potřeba mnohem více energie, ve srovnání s látkami, které mají nižší měrnou tepelnou kapacitu. Voda má vysokou tepelnou kapacitu díky silným vazbám mezi atomy vodíku v molekule vody.
Voda je jednou z hlavních složek všech živých organismů a rostlin na Zemi, proto její měrná tepelná kapacita hraje důležitou roli pro život na naší planetě. Vzhledem k vysoké měrné tepelné kapacitě vody se teplota kapaliny v rostlinách a teplota dutiny v těle živočichů jen málo mění i ve velmi chladných nebo velmi horkých dnech.

Voda poskytuje systém pro udržení tepelného režimu jak u živočichů a rostlin, tak na povrchu Země jako celku. Obrovská část naší planety je pokryta vodou, takže voda hraje velkou roli při regulaci počasí a klimatu. I při velkém množství tepla přicházejícího v důsledku vlivu slunečního záření na zemský povrch se teplota vody v oceánech, mořích a dalších vodních plochách postupně zvyšuje a pomalu se mění i okolní teplota. Na druhou stranu vliv intenzity tepla ze slunečního záření na teplotu je velký na planetách bez velkých povrchů pokrytých vodou, jako je Země, nebo v oblastech Země, kde je vody vzácné. To je zvláště patrné, když se podíváte na rozdíl mezi denními a nočními teplotami. Například u oceánu je rozdíl mezi denními a nočními teplotami malý, ale v poušti je obrovský.
Vysoká tepelná kapacita vody také znamená, že se voda nejen pomalu ohřívá, ale také pomalu ochlazuje. Díky této vlastnosti se voda často používá jako chladivo, tedy jako chladivo. Kromě toho je výhodné používat vodu kvůli její nízké ceně. V chladném klimatu cirkuluje horká voda v potrubí pro vytápění. Ve směsi s etylenglykolem se používá v chladičích automobilů k chlazení motoru. Takové kapaliny se nazývají nemrznoucí kapaliny. Tepelná kapacita etylenglykolu je nižší než tepelná kapacita vody, takže tepelná kapacita takové směsi je také nižší, což znamená, že účinnost chladicího systému s nemrznoucí směsí je také nižší než u systému s vodou. Ale musíte se s tím smířit, protože etylenglykol zabraňuje zamrznutí vody v zimě a poškození kanálů chladicího systému automobilu. Do chladicích kapalin určených pro chladnější klima se přidává více etylenglykolu.
Tepelná kapacita v každodenním životě
Jsou-li všechny ostatní věci stejné, tepelná kapacita materiálů určuje, jak rychle se zahřejí. Čím vyšší je měrné teplo, tím více energie je potřeba k ohřevu tohoto materiálu. To znamená, že pokud se dva materiály s různými tepelnými kapacitami ohřívají stejným množstvím tepla a za stejných podmínek, pak se látka s nižší tepelnou kapacitou zahřeje rychleji. Materiály s vysokou tepelnou kapacitou se naopak zahřívají a uvolňují teplo zpět do okolí pomaleji.

Kuchyňské náčiní a nádobí
Nejčastěji vybíráme materiály na nádobí a kuchyňské náčiní podle jejich tepelné kapacity. Týká se to především předmětů, které přicházejí do přímého kontaktu s teplem, jako jsou hrnce, talíře, zapékací misky a další podobné náčiní. Například pro hrnce a pánve je lepší používat materiály s nízkou tepelnou kapacitou, jako jsou kovy. To napomáhá snadnějšímu a rychlejšímu přenosu tepla z ohřívače přes pánev do jídla a urychluje proces vaření.
Na druhou stranu, protože materiály s vysokou tepelnou kapacitou udrží teplo dlouho, je dobré je použít k izolaci, tedy když je potřeba teplo výrobků udržet a zabránit jeho úniku do okolí nebo naopak , aby se zabránilo ohřevu chlazených produktů teplem v místnosti. Nejčastěji se takové materiály používají na talíře a šálky, ve kterých se podávají teplé nebo naopak velmi studené pokrmy a nápoje. Pomáhají nejen udržovat teplotu produktu, ale také zabraňují popálení lidí. Keramické nádobí a nádobí z expandovaného polystyrenu jsou dobrým příkladem použití takových materiálů.

Izolační potravinářské výrobky
V závislosti na řadě faktorů, jako je obsah vody a tuku v potravinách, se liší jejich tepelná kapacita a měrná tepelná kapacita. Při vaření umožňuje znalost tepelné kapacity potravin použít některé produkty k izolaci. Umístění izolačních výrobků na jiné potraviny pomůže potravinám pod nimi udržet teplo déle. Pokud má nádobí pod těmito tepelně izolačními produkty vysokou tepelnou kapacitu, pak pomalu uvolňuje teplo do okolí. Jakmile se dobře zahřejí, ztrácejí teplo a vodu ještě pomaleji díky izolačním produktům nahoře. Proto zůstávají déle horké.
Příkladem tepelně izolační potraviny je sýr, zejména na pizze a dalších podobných pokrmech. Dokud se nerozpustí, umožňuje průchod vodní páře, což umožňuje potravinám pod ní rychle vychladnout, protože voda, kterou obsahuje, se vypařuje, a tím ochlazuje potraviny, které je obsahují. Roztavený sýr pokrývá povrch misky a izoluje jídlo pod ním. Sýr často obsahuje potraviny s vysokým obsahem vody, jako jsou omáčky a zelenina. Díky tomu mají vysokou tepelnou kapacitu a dlouho udrží teplo, zejména proto, že jsou pod taveným sýrem, který nepropouští vodní páru. To je důvod, proč pizza vychází z trouby tak horká, že se můžete snadno spálit omáčkou nebo zeleninou, i když těsto na okrajích již vychladlo. Povrch pizzy pod sýrem dlouho nevychladne, což umožňuje doručit pizzu až domů v dobře izolované termotašce.

Některé recepty používají omáčky stejným způsobem jako sýr, aby izolovaly jídlo pod ním. Čím vyšší obsah tuku v omáčce, tím lépe izoluje jídlo – omáčky na bázi másla nebo smetany jsou v tomto případě obzvlášť dobré. Je to opět způsobeno tím, že tuk zabraňuje odpařování vody a tím i odběru tepla potřebného k odpařování.
Při vaření se někdy k tepelné izolaci používají materiály, které nejsou vhodné pro potraviny. Kuchaři ve Střední Americe, na Filipínách, v Indii, Thajsku, Vietnamu a mnoha dalších zemích k tomuto účelu často používají banánové listy. Dají se nejen nasbírat na zahrádce, ale i koupit v obchodě nebo na trhu – dokonce se pro tyto účely dováží i do zemí, kde se banány nepěstují. Někdy se pro izolační účely používá hliníková fólie. Zabraňuje nejen odpařování vody, ale také pomáhá zadržovat teplo uvnitř tím, že zabraňuje přenosu tepla ve formě sálání. Pokud křídla a další vyčnívající části ptáčka při pečení zabalíte do alobalu, alobal zabrání jejich přehřátí a připálení.
Vaření
Potraviny s vysokým obsahem tuku, jako jsou sýry, mají nízkou tepelnou kapacitu. Zahřívají se více s menší energií než potraviny s vysokou tepelnou kapacitou a dosahují dostatečně vysokých teplot, aby došlo k Maillardově reakci. Maillardova reakce je chemická reakce, ke které dochází mezi cukry a aminokyselinami a mění chuť a vzhled potravin. Tato reakce je důležitá při některých způsobech vaření, jako je pečení chleba a pečiva z mouky, pečení jídel v troubě a smažení. Pro zvýšení teploty potravin na teplotu, při které k této reakci dochází, se při vaření používají potraviny s vysokým obsahem tuku.
Cukr při vaření


Měrné teplo cukru je ještě nižší než u tuku. Protože se cukr rychle zahřeje na teploty vyšší než je bod varu vody, práce s ním v kuchyni vyžaduje dodržování bezpečnostních pravidel, zejména při přípravě karamelu nebo cukroví. Při tavení cukru musíte být velmi opatrní a nerozsypat jej na nechráněnou pokožku, protože teplota cukru dosahuje 175 °C (350 °F) a popálení od roztaveného cukru bude velmi vážné. V některých případech je nutné zkontrolovat konzistenci cukru, ale nikdy by se to nemělo dělat holýma rukama, pokud je cukr zahřátý. Lidé často zapomínají, jak rychle a jak horký cukr se dokáže zahřát, a proto se spálí. V závislosti na tom, k čemu je roztavený cukr určen, lze jeho konzistenci a teplotu zkontrolovat pomocí studené vody, jak je popsáno níže.

Vlastnosti cukru a cukrového sirupu se mění v závislosti na teplotě, při které se vaří. Horký cukrový sirup může být řídký, jako ten nejtenčí med, hustý nebo někde mezi řídkým a hustým. Recepty na bonbóny, karamely a sladké omáčky obvykle specifikují nejen teplotu, na kterou se má cukr nebo sirup zahřát, ale také stupeň tvrdosti cukru, jako je fáze „měkká kulička“ nebo fáze „tvrdá kulička“. . Název každé fáze odpovídá konzistenci cukru. Pro určení konzistence cukrář nakape několik kapek sirupu do ledové vody a ochladí je. Poté se konzistence zkontroluje dotykem. Pokud tedy například vychlazený sirup zhoustne, ale neztuhne, ale zůstane měkký a lze jej tvarovat do koule, pak se sirup považuje za fázi „měkké koule“. Pokud je tvar mraženého sirupu velmi obtížný, ale přesto jej lze ručně změnit, pak je ve fázi „tvrdé koule“. Cukráři často používají potravinářský teploměr a také ručně kontrolují konzistenci cukru.

Bezpečnost potravin

Znáte-li tepelnou kapacitu produktů, můžete určit, jak dlouho je třeba je chladit nebo ohřívat, aby dosáhly teploty, při které se nezkazí a při které se zabíjejí bakterie škodlivé pro tělo. Například, aby potraviny s vyšší tepelnou kapacitou dosáhly určité teploty, trvá déle, než se ochladí nebo ohřejí, než potraviny s nízkou tepelnou kapacitou. To znamená, že doba vaření pokrmu závisí na tom, jaké produkty jsou v něm obsaženy, a také na tom, jak rychle se z něj odpařuje voda. Odpařování je důležité, protože vyžaduje hodně energie. Ke kontrole, na jakou teplotu se pokrm nebo jídlo v něm zahřálo, se často používá potravinářský teploměr. Je zvláště vhodné jej používat při vaření ryb, masa a drůbeže.
Mikrovlnné trouby
Jak efektivně mikrovlnná trouba ohřívá jídlo, závisí mimo jiné na specifické tepelné kapacitě jídla. Mikrovlnné záření produkované magnetronem mikrovlnné trouby způsobuje, že molekuly vody, tuku a některých dalších látek se pohybují rychleji, což způsobuje ohřívání jídla. Molekuly tuku se snadno pohybují díky jejich nízké tepelné kapacitě, proto tučná jídla dosahují vyšších teplot než potraviny, které obsahují hodně vody. Dosažená teplota může být tak vysoká, že je dostatečná pro Maillardovu reakci. Výrobky s vysokým obsahem vody nedosahují kvůli vysoké tepelné kapacitě vody takových teplot, a proto v nich nedochází k Maillardově reakci.
Vysoké teploty, kterých dosahuje tuk v mikrovlnné troubě, mohou křupat některá jídla, jako je slanina, ale tyto teploty mohou být při používání mikrovlnné trouby nebezpečné, zvláště pokud se neřídíte návodem k použití v návodu k použití trouby. Například při ohřívání nebo vaření tučných jídel v troubě byste neměli používat plastové nádobí, protože ani nádobí do mikrovlnné trouby není navrženo tak, aby vydrželo teploty, kterých tuk dosáhne. Měli byste také pamatovat na to, že tučná jídla jsou velmi horká a jezte je opatrně, abyste se nespálili.
Měrná tepelná kapacita materiálů používaných v každodenním životě
Je pro vás obtížné překládat měrné jednotky z jednoho jazyka do druhého? Kolegové jsou připraveni vám pomoci. Zadejte dotaz v TCTerms a během několika minut dostanete odpověď.
S pojmem „specifické teplo“ se v hodinách fyziky setkává každý školák. Ve většině případů lidé zapomínají na školní definici a často vůbec nerozumí významu tohoto pojmu. Na technických univerzitách se většina studentů dříve či později setká s měrnou tepelnou kapacitou. Možná v rámci studia fyziky nebo možná někdo bude mít takový obor jako „tepelné inženýrství“ nebo „technická termodynamika“. V tomto případě si budete muset zapamatovat školní osnovy. Níže je tedy uvedena definice, příklady a významy některých látek.
Definice
Měrná tepelná kapacita je fyzikální veličina, která charakterizuje, jaké množství tepla je třeba dodat nebo odebrat jednotce látky, aby se její teplota změnila o jeden stupeň. Je důležité zrušit, že na tom nezáleží, stupně Celsia, Kelvina a Fahrenheita, hlavní je změna teploty po jednotkách.
Měrná tepelná kapacita má svou vlastní měrnou jednotku - v mezinárodní soustavě jednotek (SI) - Joule, děleno součinem kilogramu a stupně Kelvina, J/(kg K); nesystémová jednotka je poměr kalorií k součinu kilogramu a stupně Celsia, cal/(kg °C). Tato hodnota se nejčastěji označuje písmenem c nebo C, někdy se používají indexy. Například, pokud je tlak konstantní, pak index je p, a pokud je objem konstantní, pak v.
Variace definice
Existuje několik formulací definice diskutované fyzikální veličiny. Kromě výše uvedeného je přijatelná definice, že měrná tepelná kapacita je poměr tepelné kapacity látky k její hmotnosti. V tomto případě je nutné jasně pochopit, co je „tepelná kapacita“. Tepelná kapacita je tedy fyzikální veličina, která ukazuje, kolik tepla se musí tělu (látce) dodat nebo odebrat, aby se jeho teplota změnila o jedničku. Měrná tepelná kapacita hmotnosti látky větší než kilogram se stanoví stejným způsobem jako u jedné hodnoty.
Některé příklady a významy pro různé látky

Experimentálně bylo zjištěno, že tato hodnota je pro různé látky různá. Například měrná tepelná kapacita vody je 4,187 kJ/(kg K). Největší hodnota této fyzikální veličiny pro vodík je 14,300 kJ/(kg K), nejmenší pro zlato je 0,129 kJ/(kg K). Pokud potřebujete hodnotu pro konkrétní látku, musíte si vzít referenční knihu a najít odpovídající tabulky a v nich - hodnoty, které vás zajímají. Moderní technologie však umožňují výrazně urychlit proces vyhledávání - stačí použít jakýkoli telefon, který má možnost přihlásit se do World Wide Web, zadat do vyhledávacího pole otázku, která vás zajímá, začít hledat a hledat za odpověď na základě výsledků. Ve většině případů musíte následovat první odkaz. Někdy však není potřeba chodit vůbec jinam – odpověď na otázku je vidět ve stručném popisu informace.

Nejběžnější látky, pro které se hledá tepelná kapacita, včetně měrného tepla, jsou:
- vzduch (suchý) - 1,005 kJ/(kg K),
- hliník - 0,930 kJ/(kg K),
- měď - 0,385 kJ/(kg K),
- ethanol - 2,460 kJ/(kg K),
- železo - 0,444 kJ/(kg K),
- rtuť - 0,139 kJ/(kg K),
- kyslík - 0,920 kJ/(kg K),
- dřevo - 1 700 kJ/(kg K),
- písek - 0,835 kJ/(kg K).